燃料電池の原理についての以下の一連の文章で、(a)~(d)に入る数式を答えなさい。物理量を示す記号は、この問題中で共通で、文中に現れるもののみを用いなさい。
神戸大学大学院 電気電子工学専攻 電力工学2021より引用
- 燃料電池で得られる電気エネルギーは、ギブスの自由エネルギーで考える。ギブスの自由エネルギーは、\(G=H-TS\)で定義される。ここで、\(H\)はエンタルピーで、内部エネルギー\(U\)、圧力\(P\)、体積\(V\)を用いて、\(H=(a)\)と表される。また、\(T\)と\(S\)は、それぞれ温度とエントロピーである。等温、等圧の条件で\(G\)の変化\(dG\)を考えれば、\(U,V,S\)それぞれの変化を\(dU,dV,dS\)として、\(dG=(b)\)となる。(*)
- 熱力学第一法則において、与える熱量を\(dQ’\)とする。また、外部への仕事は力学的仕事\(PdV\)と電気的仕事\(dW_{e}’\)の和とする。すると、法則は\(dU=(c)\)と表される。(**)
- (**)式を用いると、(*)式は\(dG+dW’_{e}=(d)\)となる。熱力学第二法則から(d)≦0なので、\(dW’_{e}≦-dG\)となり、外部へ電気的仕事を取り出すには、それより大きな\(-dG\)、つまり\(G\)の減少が必要である。よって、燃料電池の最大出力は、ギブスの自由エネルギーの減少分である。
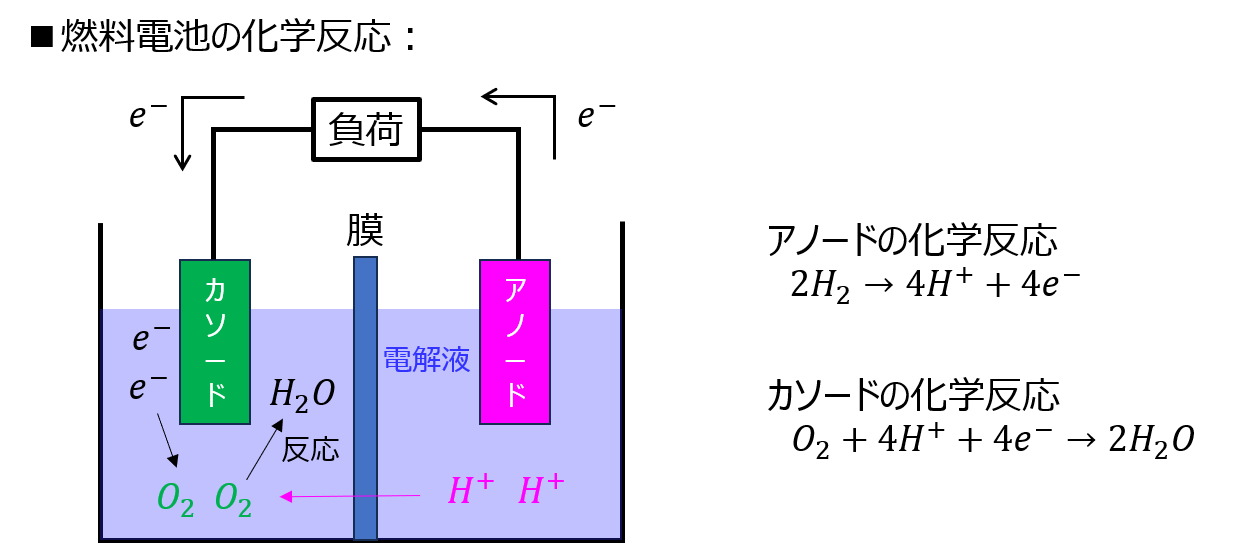
燃料電池とは
酸素と水素の化学反応により、水を生成したときの差分の電気エネルギーを動力として取り出す発電装置です。
酸素は大気中に存在しており、容易に取り出すことができます。
燃料となる水素をタンクに貯めておいて電気が必要な時に供給すれば、発電することができます。
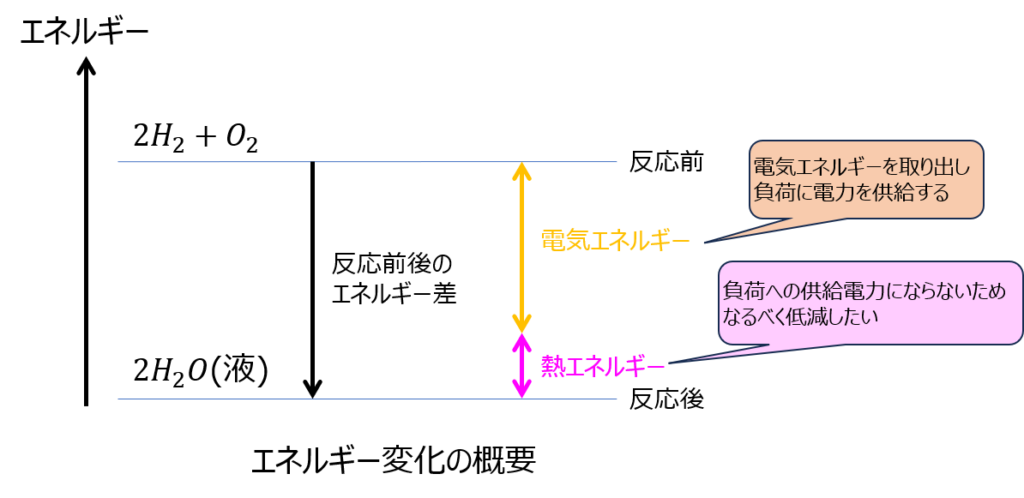
尚、発電により発生した化学エネルギーは全て電気エネルギーとして取り出せるわけではなく、一部は熱エネルギーになります。
燃料電池の理論効率
電気化学反応が発生したときのエンタルピー変化を\(\Delta H<0\)、ギブスエネルギー変化を\(\Delta G<0\)エントロピー変化を\(\Delta S <0\)とすると、理論効率\(\eta\)は
\begin{aligned}\eta=\dfrac{-\Delta G}{-\Delta H} = \dfrac{-\Delta H+T \Delta S}{-\Delta H} \fallingdotseq 0.83 \end{aligned}
となります。17%の損失は、水素と酸素が水になるときのエントロピーの減少による発熱に使われています。
燃料電池の構成
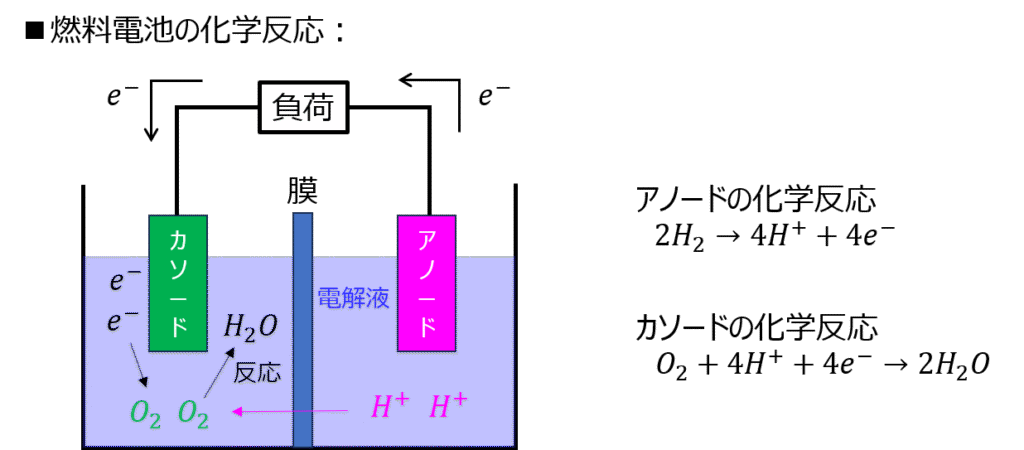
正極(アノード)と陰極(カソード)に分かれています。
正極からは水素、陰極からは酸素を供給します。
供給した水素は電解質膜を通り、陰極へたどり着きます。
陰極にて、下記の化学反応が発生し、電子が放出されます。
\begin{aligned}2H^{+}+O^{2-}→H_{2}O+2e^{-}\end{aligned}
これに電圧をかけると電力(電気エネルギー)になるわけですね。
なお、実際の燃料電池では、反応が発生しやすいように触媒(白金)がよく用いられます。
ただし、白金は高価のため、白金無しで反応効率を高める研究も盛んにおこなわれています。
燃料電池の利点
- 化学反応の過程で二酸化炭素を放出しない。(クリーンエネルギー)
- 従来の発電所に対して小型、静粛で、居住エリアに設置できる。(注意点有り)
- エネルギー効率が高い(83%)
太陽光発電の記事で述べた内容と似ていますが、エネルギー効率が高いことが最も違います。
太陽光発電の場合、日光を全て電気エネルギーに変換できないことにより、発電効率は20%程度となっています。
一方で、燃料電池の場合は電気化学の枠組み内で発電でき、エネルギー変換のロスが無いことから、発電効率が高いです。
他、大規模な発電所は、発電をするための燃料ヤードからボイラ、タービンなど大型機器が勢ぞろいです。また、回転体のため音が非常に大きいです。このため、居住エリアに易々と設置できるものでは無いです。
一方で、燃料電池の場合は、水素を貯めておくタンクの設置位置の制約はあるものの、他の機器はある程度小型です。よって、居住エリアに設置することができます。
他、大容量のエネルギーを求められる移動体(トラックなど)でも、リチウムイオンバッテリー(BEV)に対し、燃料電池(FCV)に軍配が上がります。
これは、BEVでトラックを構成する際、車体重量が大きくなり、燃費の観点で不利だからです。
(ただし、出力応答性はBEVの方が良いです。このため、走り出しの加速感ではFCVが劣ります。)
このように、バッテリーよりは大型で、従来の発電所に対しては小型の出力が求められる中型の領域にて燃料電池は使用されやすいです。
燃料電池の課題
- コストが高い
- 耐久性に難がある
- 応答性が悪い
高コスト
再生可能エネルギー全般に言えることですが、燃料電池もコストが高いです。
触媒に用いる白金および燃料電池スタックに使用するセルが高価になっています。
一方で、最近は燃料電池の多用途展開が進み、出荷数も増加していることから、全体的な価格は低下傾向になっています。今後の伸びが期待されます。
耐久性の課題
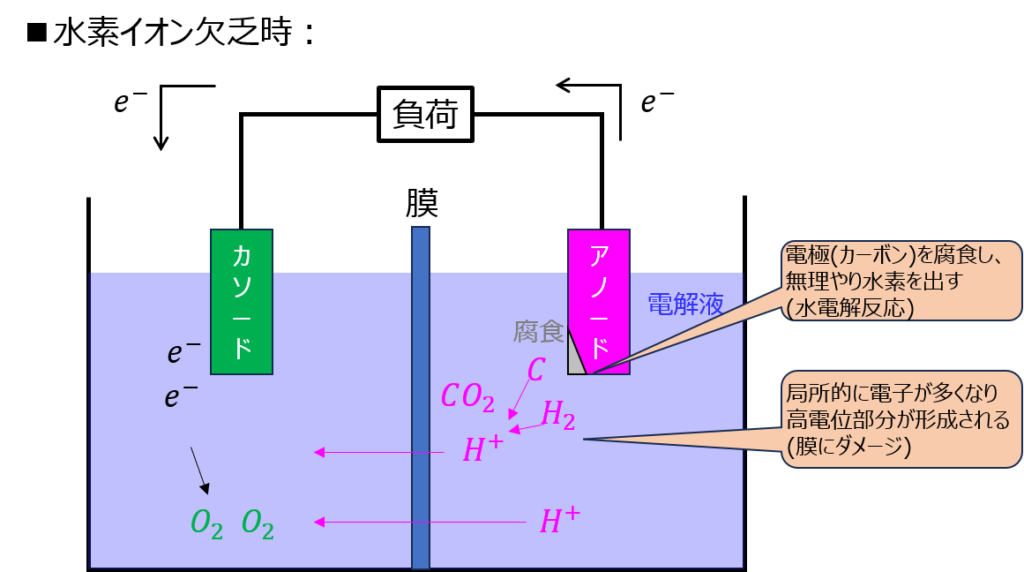
燃料電池の劣化要因としては、いくつか形態があります。一例として、水素の供給が欠乏したときセルが劣化します。
\begin{cases}H_{2}→2H^{+}+2e^{-} \\ O_{2}+4H^{+}+4e^{-}→2H_{2}O\end{cases}
通常、上記の化学反応により燃料電池は発電しますが、第一式の\(H_{2}\)が足りないとき、どこかから水素を補充必要が出てきます。
このとき、電極(炭素)で以下の反応が発生します。
\begin{aligned}C+2H_{2}O→CO_{2}+4H^{+}+4e^{-}\end{aligned}
電極が劣化し、発電性能の劣化に繋がります。
また、局所的に水電解反応が発生し、高電位部分が形成されます。この結果、膜にもダメージが入ります。
この現象は、通常運転時に発生するリスクもあります。しかし、長期間放置した後の起動時もスタック内に酸素が充満していることから発生し得る現象になっています。
いずれにせよ、スタック内に高電位が発生しないオペレーションが必要です。
応答性が悪い
燃料電池は、化学エネルギーとしての貯蔵であるため、電気エネルギーとして貯蔵するリチウムイオン電池、EDLC(電気二重層コンデンサ)と比較して応答性が悪いです。
このため、燃料電池自動車の場合、電気バッテリーと組み合わせて出力制御をすることが多いです。
一例として、加速をする際は瞬時に出力要求が大きくなるため、バッテリーからのエネルギー持ち出しが多いです。一方で、一定速度巡行をする際は、貯蔵エネルギー量の大きい燃料電池からエネルギー出力します。
このようにして、高加速力と航続距離の長さを両立します。
※実際は、燃料電池自動車だけでなく、応答性の高さと大容量性の両方を求められるシステム全般に、電気貯蔵装置と燃料電池は使用されます。
(例:電力系統に接続する需要家のデマンド変動に伴う電力補償など)
解答例
(a)エンタルピーと自由エネルギーの関係式
問題文の誘導に乗り、
\begin{aligned}H=H+PV\end{aligned}
(b)ギブスの自由エネルギーの変化量
\(G=H-TS=U+PV-TS\)を微分すると
\begin{aligned}dG=dU+PdV+VdP-TdS-SdT\end{aligned}
等温、等圧条件下では、\(dT=dP=0\)のため
\begin{aligned}dG=dU-TdS+PdV\end{aligned}
(c)熱力学第一法則から考える仕事量
過去の記事より、熱力学第一法則は\(Q=U+W\)と表される。(微分形:\(dQ=dU+dW\)も同様に成り立つ。)
問題文より、外部から受ける仕事は、力学的仕事\(PdV\)、電気的仕事\(dW_{e}\)の和で表すことができるため
\begin{aligned}dQ=dU+PdV+dW_{e} \\ dU=dQ-PdV-dW_{e}\end{aligned}
を得る。
(d)電気的仕事とギブスの自由エネルギーの関係
(c)の結果を変形し、\(PdV=dQ-dU-dW_{e}\)
これを(b)の結果に代入し、
\begin{aligned}dG&=dU-TdS+dQ-dU-dW_{e} \\ &=dQ-TdS-dW_{e}\end{aligned}
これを整理し
\begin{aligned}dG+dW_{e}=dQ-TdS\end{aligned}
参考文献
トコトンやさしい燃料電池の本 森田 敬愛(著) No4,5,6,13,39
電気エネルギー工学 八坂 保能(編著) P91~93